ロボティクスの歴史 (2022.7.7~)
日本はロボットに関わる技術・部品生産などにおいて、世界でも有数の生産国となっています。制御部品、メカニカル部品、プログラミングなど様々な産業分野の生産工場で使用されるこれらの技術や、自動車や飛行機など製品そのものにも使用されている機械的な構造など、これらの基幹技術は「機織り」や「紡績」から始まります。
製糸産業が活発になる以前より、日本において平地では稲作が行われることが多く、きれいな水が豊富で美味しいお米がよくとれる新潟、秋田、富山(東日本)、兵庫(西日本)などお米の産地はそのまま日本酒造りが盛んです。酒造りではまずお米のでんぷん分子を切り刻んで糖化するために、「室=むろ」という温湿度を管理した部屋に蒸米を広げて、少し冷めたところでその上から「こうじかび」を振りかけます。その後、温湿度を保ったまま何度かお米の上下を入れ替え、ほぐすことで好気性であるこうじかびはお米の内部にまで菌糸を伸ばして増殖し、でんぷんを切り刻む酵素=アミラーゼを作り始めます。これによりお米が糖化して、次の工程となる「もろみ」において酵母が糖(ぶどう糖)をエタノールに替えていきます。これは発酵の一種です。同じく発酵により作り出される食品には醤油があります。ここでもこうじかびが利用されていますが、醬油の産地は千葉、小豆島、和歌山、兵庫など海沿いの地域が多いようです。これは塩が入手しやすいことも関係していますが、最も重要なのは温暖な気候と湿度です。
これに対して、海から離れた内陸の山間地帯、特に上野国、信濃国や甲斐国などでは養蚕が盛んに行われてきました。絹糸を吐き出し繭をつくる「カイコ」は、室温が暖かい状態でかつ桑の葉が柔らかく保てる湿度環境におくと食勢がよくなり成長も早くなります。しかしながら、この高温多湿環境は上述のようにカイコの最大の敵となる「こうじかび病」が発生しやすいため、日本酒造りと養蚕は自然に住み分けがなされてきました。養蚕農家が内陸に多いのは、雨が少なく乾燥していて湿度の制御がしやすいため、かびから逃れる環境をつくりやすい、ことが大きな要因だと考えられます。
このような背景のもと、上野国、信濃国と甲斐国の中間地点に、日本としては全ての産業において初めての近代的な工場となる「富岡製糸場」が国費で建設されました。この時代はまだ電気が無かったため、回転動力は蒸気機関や人力で行われていました。蒸気機関は石炭を使用するため、近くに炭鉱があるということもこの場所が選ばれた理由の一つであることでしょう。
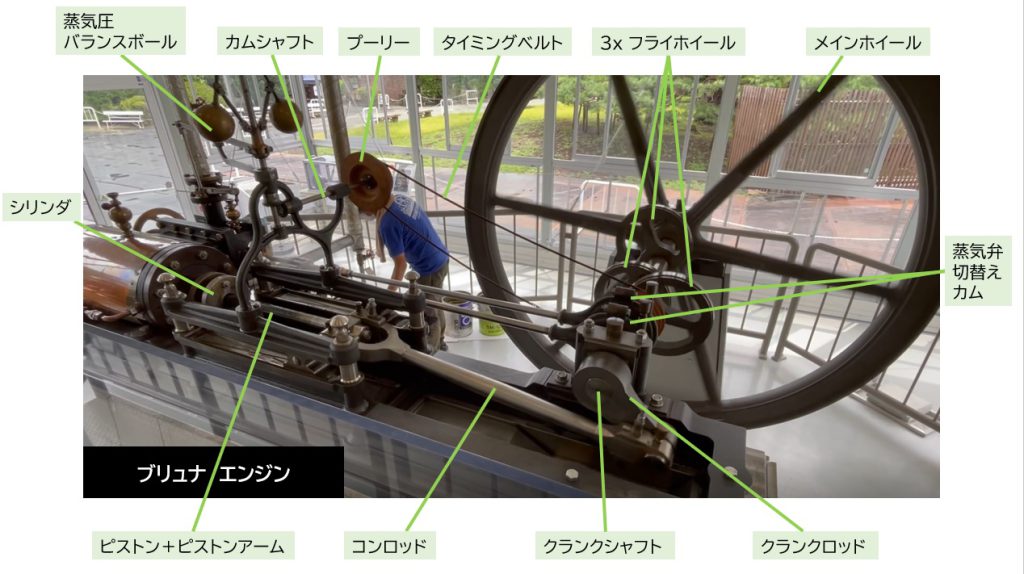
絹糸を繭から木製(あるいは金属製)の糸車に巻き取る工程を繰糸(そうし)と言いますが、この作業を一度に多数かつ半自動(自動で巻きながら人が手助けする)で行うために、蒸気機関(図1)から得た回転動力を非常に長い円筒軸にゴム製のベルトで伝達することで、数十メートルにわたってこの作業を実現させる事ができました。図2にある富岡製糸場の繰糸場では最下部に「繭を煮る窯」、中間下部に糸をよりながらまとめる「糸より機構」、中間上部に巻き糸が片寄らないようにするための「左右往復部」、最上部に糸を巻きとる「糸車」が配置してあるのが見て取れます。巻き取りの動力のみではなく、左右往復部の動力も蒸気機関から得た回転動力とばね力などを用いて得ていたと思われます。
図1:蒸気機関(ブリュナエンジンの復元機) 図2:繰糸場
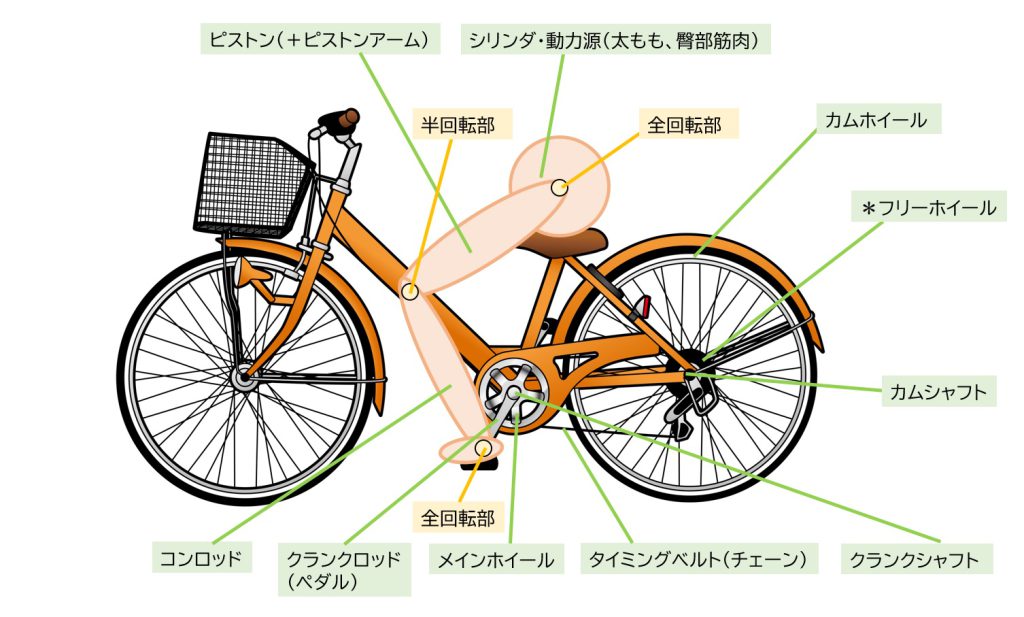
ブリュナエンジンと自転車の部品比較
このような動力を伝達するための部品として、ギヤ、ベルト、カムなどがあります。
自動化(オートメーション)とは
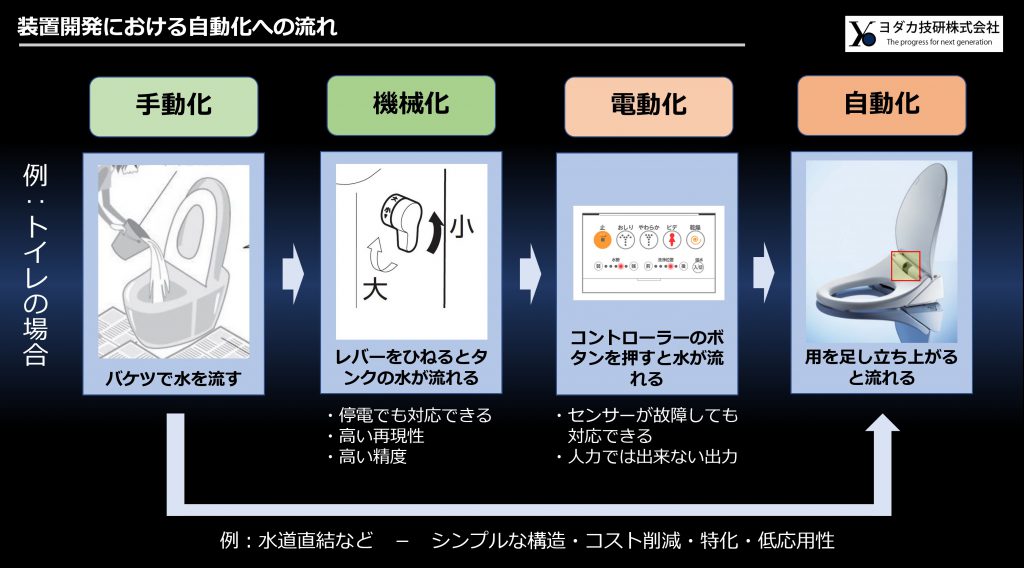
自動化を行う目的は多項目にわたりますが、一言でいえば「効率化」です。繰り返しひたすらシールを貼る作業もあれば、人が持てない重量物を高速で運ぶこともあります。いずれにしましても、世の中では一般的に「手動化 vs 自動化」ということで比較されますが、これを紐解いてみるとこの手動化と自動化の間には他にも「機械化」と「電動化」が含まれていることに、大半の人は気づいていないのではないでしょうか?
身近なところでは「トイレ」が分かりやすいので、これを例に挙げます。
手動化と聞いて、皆さんはレバーをひねることを考えましたでしょうか?実をいうとこれは「機械化」であり、手動化ではありません。手動化はバケツなどで水を直接便器に流すことになります。当然、思いバケツを抱えて、毎回トイレに行くことは容易ではありませんが、他に何もなくてもバケツの水があれば流すことはできます。
次に機械化ですが、上述しましたようにレバーをひねるとタンクの水が流れる機構、これが「機械化」です。停電でも対応できますし、バケツに比べたら毎回同じ量の水を流すこともできます。人がこのように道具を使用して操作する機構は自動化に比べて高い精度(非常に少量を流すなど)、あるいは高速に行える(連続的に何度も流せる)ことも多々あります。
続いて電動化ですが、現在のトイレはこれが多く見受けられます。コントローラーボタンを押すと水が流れる機構です。モーターを利用する場合が多く、トイレの場合はあまり必要になりませんが手動化や機械化では出すことのできないパワーを出力することができます。
最後に自動化です。自動化は人が何かの操作をしなくてもセンサーが働き、勝手に作動してくれるものになります。自動化においてセンサーが重要な部品であることは間違いないでしょう。現在はイメージセンサーが発展し、AIと絡めて様々なパラメーターを抽出・計算することで、人が介在しなくてもすべてが済む時代です。
このときに、何から何まで自動化するのではなく、一部は機械化や電動化にすることで柔軟性が高くなる、あるいは精度が上がることを認識する必要もあります。これとは反対に、現在の機械化や電動化にとらわれすぎてシンプルに済ませられることに気が付かない点も注意が必要です。トイレの場合、センサーと水道に直結したバルブが存在するだけで水を流すことが出来るようになります。仮に停電が起きた際には手動化によりバケツで流せば済む、ということもあります。
小型リニアアクチュエータ
このたび当社は「多階層ロボティクス」の実現に向けて、小型リニアアクチュエータの開発を進め、特許を出願いたしました。
近年、自動化ニーズに伴うロボット産業の発展により、「リニアアクチュエータ」の需要が増加しております。
リニアアクチュエータは、モーターの回転シャフトの同軸上に送りねじやボールネジを固定し、そのネジに取り付けてあるナットにステージを固定することで、回転運動を直動に変換する装置です。送りネジやボールネジのみで直動運動を行うと「がたつき」が発生するため、ステージの下にボールベアリングやローラーなどを使用し、ガイドレールの上を滑らせるようにすることで摩擦を低減しながら、がたつきを抑え滑らかに動くようにしています。
実使用の場合、ステージに物体を取り付け、ステージを直線的に往復運動させ、取り付けた物体を目的の位置で止めるのが主な用途となります。このリニアアクチュエータの最大の市場は様々な組立作業が行われる工場となります。
工場などの組立作業においては数kg以上の耐荷重が必要となります。この場合、先に挙げたボールベアリングやローラー、あるいはガイドレールにかかる負担が大きいためこの部分の強度を上げることが前提条件でした。これらの部品はコストや加工のしやすさの面から以前は鉄を用いて加工し「焼き入れ」や「焼き戻し」を行っていました。この作業を行う事で強度を高くし、耐久性を上げてきました。
その後、加工技術や材料技術が発展し、各部品が鉄からステンレスなどの汎用鋼に置き換わることで焼きの作業が必要なくなり、精度の向上やコスト削減につながりました。現在の電動リニアアクチュエータや電動シリンダと呼ばれるロボットの基幹部品はステンレスに置き換わっています。
しかしながら、ローラーガイドで用いられるクロスローラーやボールベアリングの仕組みは非常に精密なものであり、製造では複雑な工程を踏むため、リニアアクチュエータで用いられる部品の中で最も高額な材料となっています。また、組み立て作業においても非常に小さい転がる部品が多いなど取り扱いが難しいことがあります。小型のリニアアクチュエータになればなるほど、これらの部品では対応できなくなることが考えられます(図1)
図1 クロスローラーガイドとクロスローラー
当社はこれらを解決するために、クロスローラーの代わりにすべり性が高く、耐摩耗性が高い樹脂の角棒に置き換え、かつ従来の構造から更に小型化するための設計を行いました。これは従来のクロスローラーガイドに比べて、大幅なコストダウンとシンプルな構造化及び高精度化につながるものです(図2)
図2 リニアアクチュエータ従来構造と新規構造の外観と重量
最大ストローク25mm以上でありながら、10ナノメートルの精度実現を目指します。
今後、省エネルギー化や小型化が必要とされるロボット分野や、細胞を扱うバイオテクノロジ―研究の現場における顕微鏡の電動ステージや微細操作など様々なシーンに応用して参ります。
電動XYZマニピュレータ
マイクロスクリューポンチ
当社では上述の小型リニアアクチュエータを応用し、現在「マイクロスクリューポンチシステム」を開発しております
(理化学研究所と共同特許出願中)
ライフサイエンス研究におきまして、臓器や生体組織から1細胞を採取するニーズが高まっておりますが、今のところ「生きたまま」の細胞を正確に1個ずつ採取する手立てはありません。
臓器や生体組織はそれぞれが独立した働きを持つ必要があり、そのため形を保たなければなりませんが、そのため厚い膜や細胞外マトリックスというスポンジ構造の骨格、筋状の繊維に覆われています。これらを切り裂きながら、かつ細胞を死なさず壊さぬように1個単位で吸引する必要があります。
生体組織から1個の細胞、もしくはある共通の特徴を持った細胞塊を「採取」したいニーズとして具体的な例は、マウスなどの実験動物からいくつかの臓器(脾臓、肺、リンパ節など)に存在するある種の細胞を切り出すということが挙げられます。そして、そのような細胞の網羅的解析を行うことが可能になると、特異な部位とそれ以外の部位の機能の差が従来行われてきた実験手法で導かれた結果よりも大きな差として判明するため本質的な理解が進み、医療における創薬や診断分野の応用につながります。
例えば脾臓は、左脇腹にある造血・リンパ器官であり、老化した赤血球の破壊や、血液中の異物の処理などの免疫に関する働きを担っています。脾臓組織の大半は赤脾髄とよばれ、赤血球を満たした静脈洞で占められていますが、赤脾髄中に点在する白脾髄では、免疫細胞である樹状細胞やマクロファージ細胞が抗原を提示し、リンパ球細胞からの抗体産生が促されます。ここで起こる抗原提示などに関する免疫の機能を詳細に解析するためには、白脾髄を効率的に切り出す必要があります。
これらのマクロファージ細胞は、免疫応答に関与するのみならず、組織の再構築や炎症応答後の組織の修復などの役割も担っており、その解析は重要となります。
また、肺のうちその主要な機能を司る肺胞は、ガス交換を担う人体の生存に必須な臓器です。健康な人は、一日に約2万リットルの空気を呼吸していますが、その空気の中には有害な細菌・ウイルスや化学物質などが含まれています。これらの有害物質に対し、肺に備わっている免疫システムが正常に機能することで、感染症、がん、アレルギー、喘息などの発症を防いでいます。肺の末端に存在する肺胞(数百mm)と呼ばれる部位は、感染症のターゲットとなることがあり、ここでの生体の防御機構の解明には、肺胞のみを「採取」して解析する方法が望ましいと考えられます。
さらに、リンパ節には、B細胞などの免疫細胞の他にストローマ細胞という間質細胞が存在しており、この細胞が骨組み構造の役割を果たしています。分かりやすく言うと、柔らかいスポンジ繊維のようなものです。リンパ管を通じてリンパ節に到達した免疫細胞は、それぞれリンパ節内の違う部位に集まっていきますが、ストローマ細胞が何らかの役割を果たしながら、その種類に応じて、各免疫細胞の集まる部位が異なっていると考えられます。
脳は、主に6種類の細胞が多層構造となっていることが現在知られています。よく脳波の実験などでどの場所でどのような反応が起こっているかなどは研究がなされていますが、より詳細な部位での働きは全くと言っていいほど理解されていないのが現実です。脳の中でも大脳、小脳、脳下垂体、視床下部、海馬、あるいはそれらの器官のある特定の部位で何が行われているのか詳細を知るための解析において、解剖して取り出した器官の切片を一度ホルマリン固定したサンプルと、生き物から生のまま採取をしたサンプルでは、大いに結果が異なることが想像できます。
胚は受精卵から分割したばかりの細胞集団です。その初期の段階は卵割と呼びますが、8個~16個の卵割に至ると、各々の細胞がその時点で生体として発生していく際、どの器官になり、どの位置に配置されるかという運命づけがなされ始めます。現時点ではこの卵割内の細胞1個を切り出してくる操作は非常に困難なのですが、この1個の切り出しが可能になると「ボディプラン」の解析が進み、生物学の根本となる進化の研究や再生医療、あるいは遺伝子治療などへの応用など様々な分野への波及効果が期待できます。
特に、再生医療分野の研究発展は目覚ましいところがありますが、実際にはこのような発生過程の運命づけのメカニズムの研究がなされないと試験管内で作製した細胞や臓器は「ボディプラン」の壁を越えられずに奇形種が出来て生体から免疫を受け排除される、またはがん化してしまう可能性が指摘されており、これらを克服するため様々な腫瘍形成抑制法も開発されています。
このような課題を解決するためには卵割の中にある細胞を1個ずつ取り出し、つぶさに遺伝子発現解析を行うことが必要となります。「この細胞が」「このタイミングで」「この遺伝子が働くことで」「将来この臓器になり得る」という予測が立つことにつながり、現在判明している遺伝子配列情報のみのような「部品表」としての情報のみではなく、真の「設計図」としての情報を見出すことが可能となると考えられます。
従来、このような生の組織から1個の細胞、あるいは微小な細胞塊を吸引する作業は困難であるがために、ほとんど行われていませんでした。代わりに、顕微鏡のフォーカス機能と組み合わせた局所レーザーを用いて、ホルマリンなどで固定化されたサンプルの目的部位のみを切り取る「レーザーマイクロダイセクション」が使用されてきました。
このような固定化サンプルのレーザーでの切り出しは確かに目的の物を切り取ることができるが、これは生きた状態とはかけ離れているため、特にタンパク質や代謝物の情報については信頼性が欠けます。
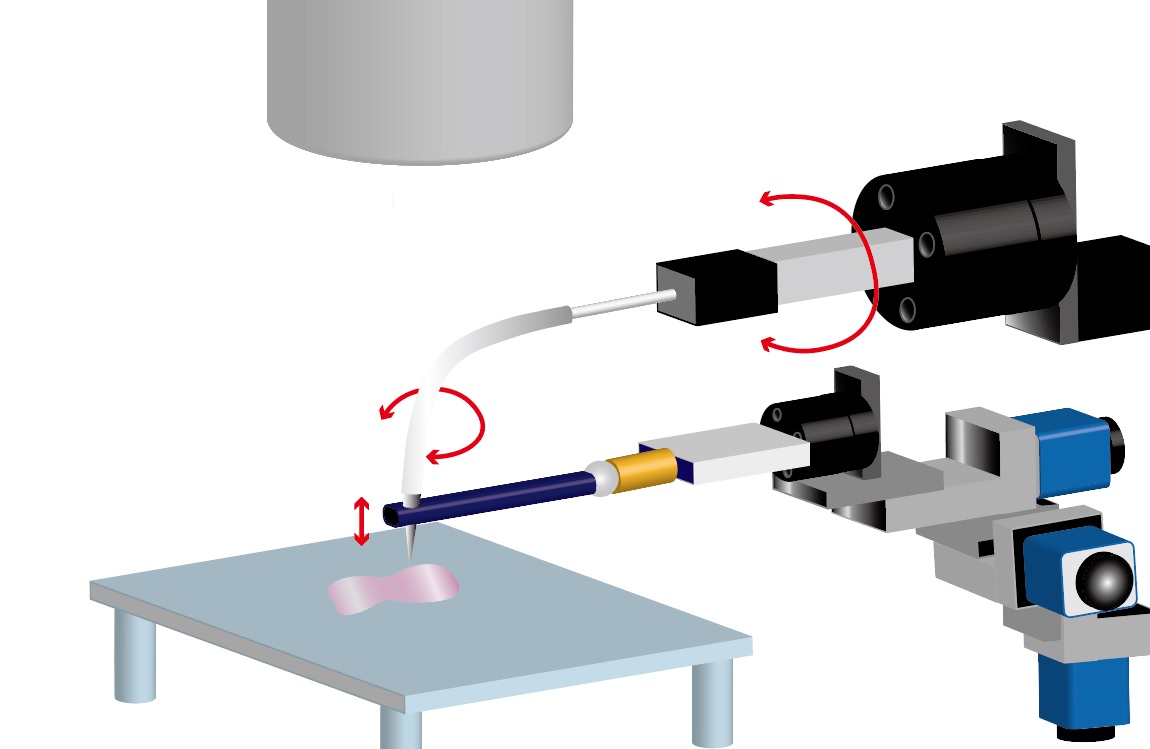
このような背景の中、市場のニーズに応えるために、当社はガラス微細管と微小液量の吸引ポンプを用いて、「採取」作業を長年にわたって行ってきました。実際には現在の技術では目的の細胞のみを採取することは非常に困難ですが、当社は小型の超微小液量操作技術(TOPickポンプ・EOポンプ)と多軸モーター制御技術(小型リニアアクチュエータ)、微細ニードル製造技術、マイクロデバイス技術を駆使して、細胞1個のハンドリングを実現するためのシステム開発を進めます。
パーソナル自動分注機
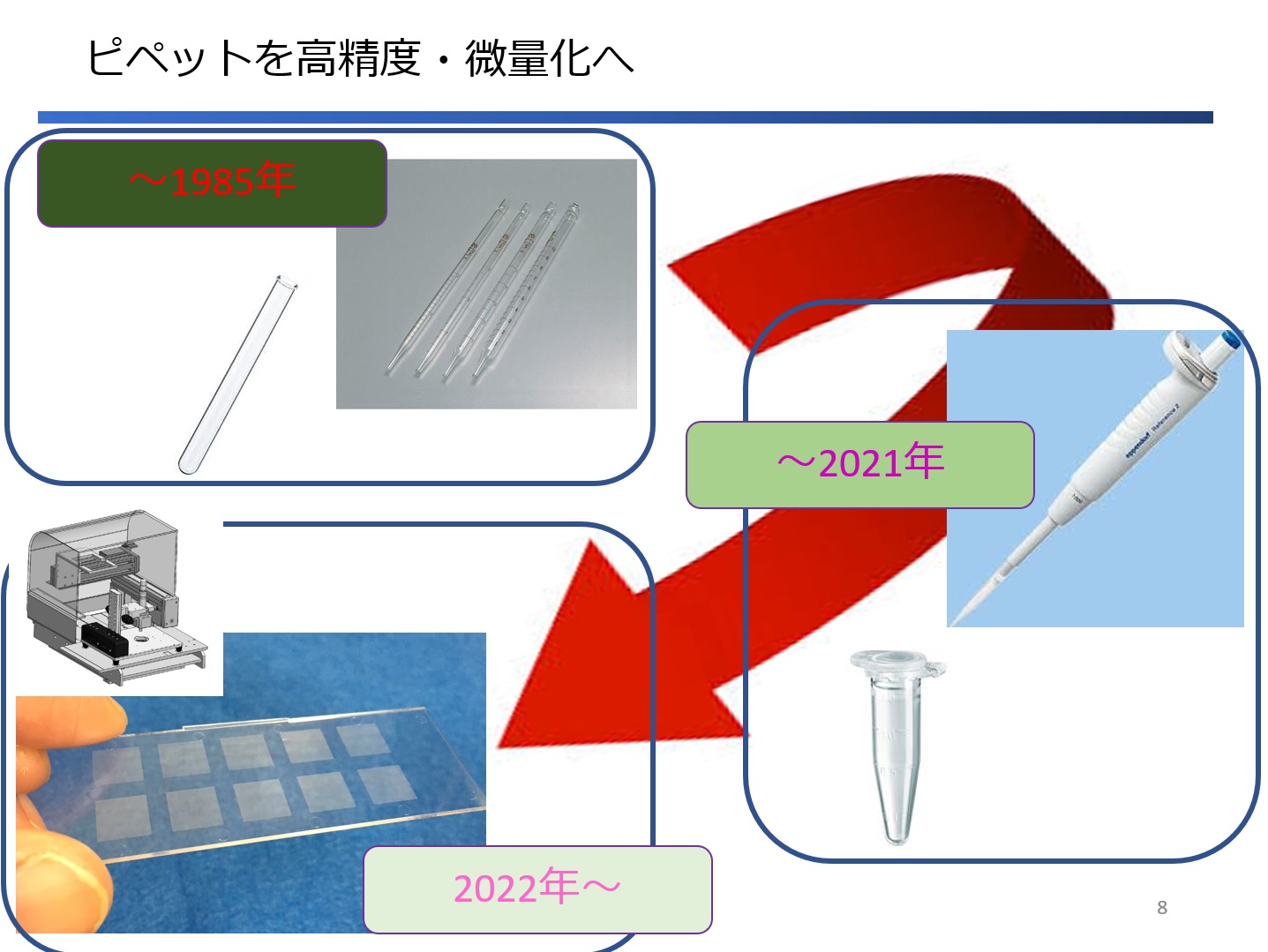
生化学・化学の研究は、取り扱う成分のほとんどが液体溶解するものであるが故に、液体操作が最も基盤となる技術となります。1970年代まではホールピペット:取り扱い液量は=mL、その後は、ギルソン社やエッペンドルフ社のマイクロピペットの開発、ヌンク社のマイクロウェルプレートの開発により取り扱い液量は=μLとなりました。これに加えてコンピューターの進歩とともに多検体スクリーニングによるデータベース化へと研究が変遷していきました。
これにより、研究結果は「再現性」という名のもと「質より量」が求められるようになり、論文の審査や米国FDA、あるいは日本の厚生労働省でも食品や医薬品の安全性に認可を付与するときに、その点を重要視するようになります。
しかしながら、そのような「質より量」を求める手法が、あたかも進んでいるように見えていた生化学研究の進歩を滞らせている主要因となっていることは、ほとんどの人が気が付いていないのが現状です。
生化学・化学研究は料理のレシピのようなものです。かといって、小さじ一杯(5g)・大さじ一杯(15g)と現在の研究では1サンプルあたりにそこまで多くの量を取り扱うことは無く、マイクロピペットを用いて100μL(水だと0.1g)、10μL(0.01g)、あるいは1μL(0.001g)という料理とは比較にならない微量液量を各容器に分注していきます。この時、実際に容器に入っている液量は、個人差によっても、ピペットによっても異なり、小さじ一杯で量る精度(実際に量りたい数値からのずれ範囲)は、それこそ料理の目分量とほとんど変わらないか、はるかに精度が劣ることもしばしば起こります。これは根本的に上述したような「質より量」を求めるところに原因があります。量をこなさなければならないため疲れてくることもあるでしょうし、または性格的に細かい作業が苦手な人である場合もあります。
そこで、人に代わり「分注ロボット」という装置を用いて、溶液の定量的な吸引・吐出を次々と連続的に各容器に行います。分注ロボットは人とは違い、疲れを知らないため、連続的に同じ条件で分注を行ってくれます。ただ、これは諸刃の剣のような局面も合わせ持ち、人では気が付く普段と違う溶液の変化も見逃してしまい、それでも止まらず同条件の分注を繰り返していってしまいます。また、分注ロボットは比較的高額な装置です。その中でも最高グレードの装置は軽く1000万円を超えますが、その精度(CV値)は±5%以下と必ずしも精度が高いとは言えません。また、取り扱う液量が微量になればなるほど、当然ながら精度が低下します。
このような精度の低下は、実験データがばらつくことなどに影響を及ぼします。このようにデータがばらつかないようにするためには量を増やすなどの変更を行うことになります。
考え方に、同じデータでなければいけないという強迫観念のようなバイアスがかかります。また、このことは新しい発見を見逃すことにつながります。
これらの課題を解決するために、マイクロピペットに代わるパーソナルな分注機が必要となりますが、今まではそれを実現するための材料や装置が高額であるがゆえに実現しておりませんでした。
今回の小型リニアアクチュエータの開発を皮切りに、2022年度の上市を目標にパーソナル自動分注機の開発に努めます。